胰腺癌(pancreatic cancer,PC)是惡性程度最高的消化系統腫瘤。由于其早期缺乏特異性的臨床表現,大多患者因癥狀出現就診時腫瘤已經擴散或轉移,確診后 5 年生存率低于 8%[1]。PC 近年來在全球范圍內均呈快速上升趨勢。2018 年美國預計新發 PC 患者 5.5 萬例,因其死亡人數達 4.4 萬例[2];預計到 2030 年,PC 將成為美國第二大癌癥死亡原因[3]。我國國家癌癥中心發布的最新數據也顯示中國 PC 發病率上升到惡性腫瘤的第十位,癌癥相關死亡率位于第六位[1]。雖然普通人群的體檢意識不斷增強,診斷技術不斷提高,但大部分 PC 發現時已是不可切除的晚期。中國的《PC 診治指南(2014)》指出對于不可切除的局部進展期或轉移性胰腺癌,積極的化學治療有助于緩解癥狀,延長生存期及改善生活質量;并推薦使用以吉西他濱(gemcitabine,GEM)為基礎的化療方案[4]。近年來已有研究[5, 6]表明 GEM 聯合化療優于標準的 GEM 單藥化療,GEM 聯合化療將是今后治療 PC 的希望與方向。同時,與卡培他濱(capecitabine,CAP)相關的進展期 PC 化療臨床試驗亦廣泛開展,而不同研究結論尚存在差異[7, 8]。本研究旨在系統評價 CAP 聯合 GEM 化療是否能在毒副反應可控的前提下顯著提高進展期 PC 的治療效果,為臨床治療胰腺癌提供參考。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型
CAP 聯合化療方案與非 CAP 聯合化療方案治療晚期 PC 的隨機對照試驗(RCT)。
1.1.2 研究對象
① 均是經病理學或細胞學檢查證實的Ⅲ~Ⅳ期(進展期或轉移)胰腺癌患者;② 年齡≥18 歲,性別不限;③ ECOG 評分為 0~2 分,或 Kamofsky 評分≥60 分。
1.1.3 干預措施
試驗組采用 CAP 聯合方案治療;非 CAP 聯合化療方案采用 GEM 單藥或含 GEM 的聯合方案治療。兩組除試驗組含 CAP 外,其他化療藥物在兩組間一致。
1.1.4 結局指標
① 中位生存期;② 疾病無進展生存期;③ 治療總有效率(CR+PR);④ 1 年生存率;⑤ 3~4 級毒副反應。
1.1.5 排除標準
① 非中、英文文獻;② 同時患第二種惡性腫瘤者;③ 1 個月內接受其他的抗癌治療;④ 預計生存期<3 個月者。
1.2 文獻檢索策略
計算機檢索 PubMed、The Cochrane Library、WanFang Data 和 CNKI 數據庫,搜集 CAP 聯合化療方案與不含 CAP 的化療方案比較治療晚期 PC 的 RCT,檢索時限均從建庫至 2017 年 12 月 1 日。此外,追溯納入文獻的參考文獻,以補充獲取相關文獻。檢索采取主題詞和自由詞相結合的方式。英文檢索詞包括:gemcitabine、capecitabine、pancreatic cancer、pancreatic carcinoma;中文檢索詞包括:吉西他濱、卡培他濱、胰腺癌。以 PubMed 為例,其具體檢索策略見框 1。

1.3 文獻篩選和資料提取
由 2 位評價員獨立篩選文獻、提取資料并交叉核對,如遇分歧,則咨詢第三方協助判斷,缺乏的資料盡量與作者聯系予以補充。文獻篩選時首先閱讀文題和摘要,在排除明顯不相關的文獻后,進一步閱讀全文,以確定最終是否納入。資料提取內容主要包括:① 納入研究的基本信息,包括研究題目、第一作者、發表雜志和時間等;② 研究對象的基線特征,包括各組樣本數、患者年齡、性別和疾病狀況等;③ 干預措施的具體細節、隨訪時間等;④ 偏倚風險評價的關鍵要素;⑤ 所關注的結局指標和結果測量數據。
1.4 納入研究的偏倚風險評價
由 2 名評價員按照 Cochrane 手冊針對 RCT 的偏倚風險評價工具評價納入研究的偏倚風險[9]。
1.5 統計分析
采用 RevMan 5.3 軟件進行 Meta 分析。采用 RR 和 HR 作為效應指標,各效應量均給出其點估計值和 95%CI。納入研究結果間的異質性采用 χ2 檢驗進行分析(檢驗水準為 α=0.1),同時結合 I2 定量判斷異質性的大小。若各研究結果間無統計學異質性,則采用固定效應模型進行 Meta 分析;若各研究結果間存在統計學異質性,則進一步分析異質性來源,在排除明顯臨床異質性的影響后,采用隨機效應模型進行 Meta 分析。明顯的臨床異質性采用亞組分析或敏感性分析等方法進行處理,或只行描述性分析。Meta 分析的檢驗水準設為 α=0.05。
2 結果
2.1 文獻篩選流程及結果
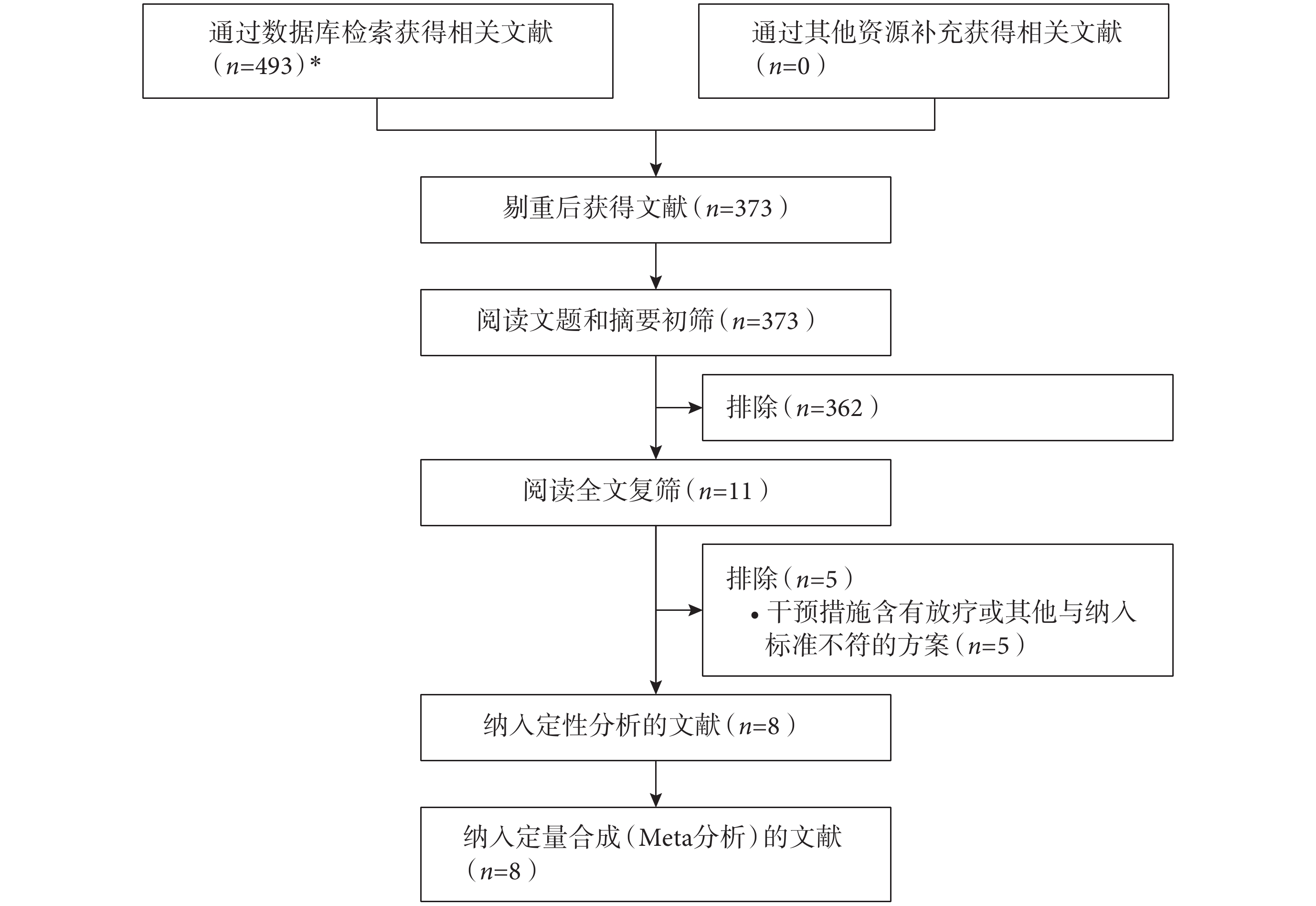
初檢出相關文獻 493 篇,經逐層篩選后,最終納入 6 個 RCT[7, 8, 10-13],共 1 317 例患者。文獻篩選流程及結果見圖 1。
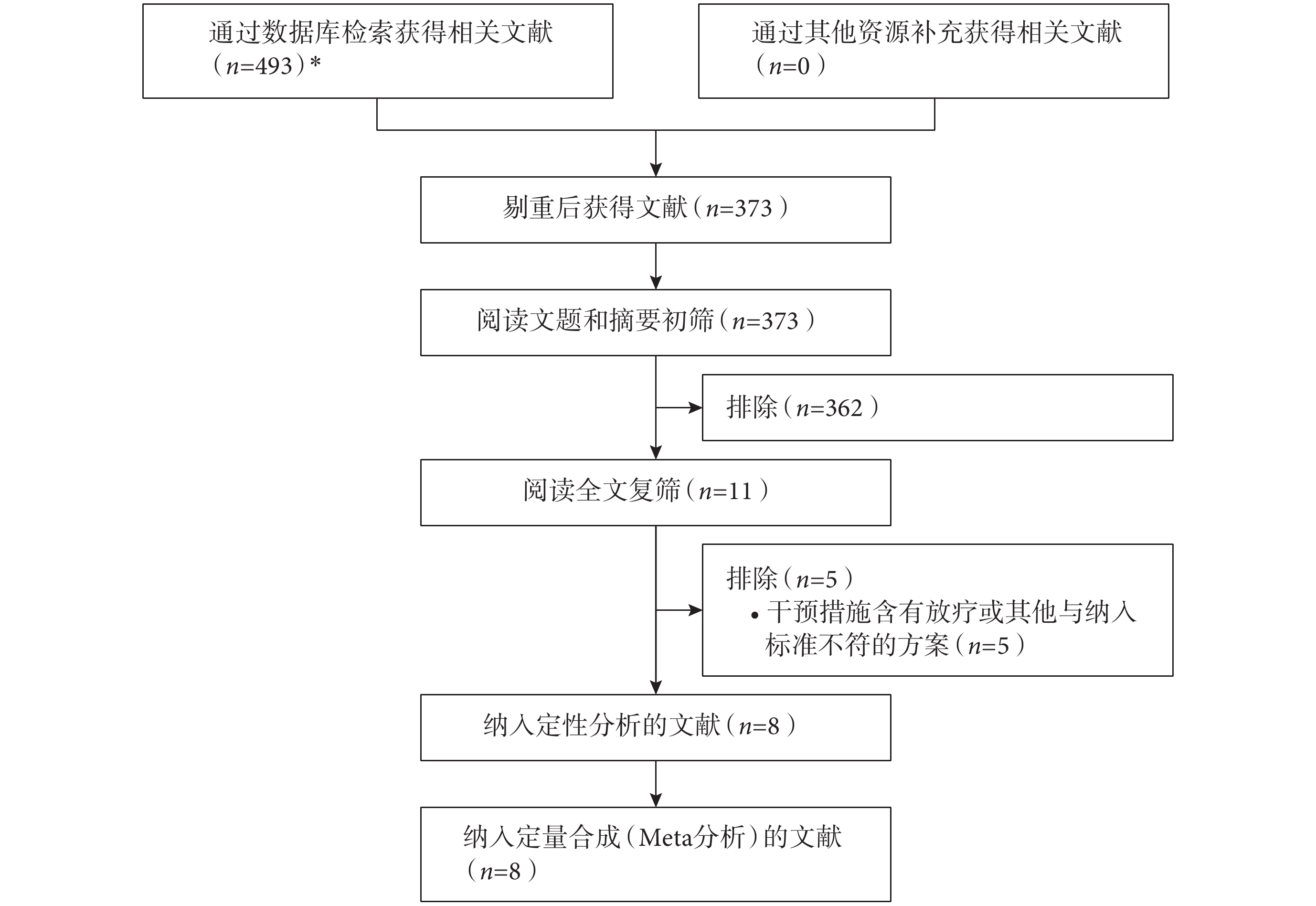 圖1
文獻篩選流程及結果
圖1
文獻篩選流程及結果
*所檢索的數據庫及檢出文獻數具體如下:PubMed(
2.2 納入研究的基本特征與偏倚風險評價結果
2.3 Meta 分析結果
2.3.1 中位生存期
共納入 5 個 RCT[7, 8, 10-12]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的中位生存期明顯優于對照組,差異有統計學意義[HR=0.86,95%CI(0.77,0.96),P=0.006](表 3)。
2.3.2 疾病無進展生存期
共納入 5 個 RCT[7, 8, 10-12]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的疾病無進展生存期明顯優于對照組,差異有統計學意義[HR=0.83,95%CI(0.75,0.91),P=0.000 2](表 3)。
2.2.3 治療總有效率
共納入 6 個 RCT[7, 8, 10-13]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的治療總有效率明顯高于對照組,差異有統計學意義[RR=1.64,95%CI(1.27,2.11),P=0.000 1](表 3)。
2.2.4 1 年生存率
共納入 3 個 RCT[10, 12, 13]。固定效應模型 Meta 分析結果顯示,兩組 1 年總生存率的差異無統計學意義[RR=1.08,95%CI(0.83,1.40),P=0.58](表 3)。
2.2.5 3~4 級毒副作用
共納入 6 個 RCT[7, 8, 10-13]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的 3~4 級中性粒細胞減少、口腔炎及手足綜合征的發生率高于非 CAP 聯合化療組(P 均<0.05)。兩組在 3~4 級貧血、血小板減少、乏力、惡心嘔吐及腹瀉方面的差異無統計學意義(P 均>0.05)(表 4)。
3 討論
晚期 PC 患者的生存時間短,目前最適合的化療方案仍不明確,急需尋找有效的化療藥物方案改善預后。以 GEM 為基礎的化療藥物治療 PC 的臨床效果確切,并為美國國立綜合癌癥網絡(NCCN)的 PC 診療指南及中國的《PC 診治指南(2014)》所推薦[4];對于不可切除的局部進展期或轉移性 PC,在全身狀況良好的情況下,采用以 GEM 或氟尿嘧啶類藥物為基礎的同步放化療或誘導化療后放療可有效緩解癥狀及改善患者預后[4]。近年來有研究報道 CAP 聯合 GEM 化療方案能夠延長晚期 PC 患者的疾病無進展生存期,但部分研究結果并不一致;因此我們將相關研究結果進行了系統評價。
本研究共納入 6 個 RCT,含 1 317 例晚期 PC 患者。Meta 分析結果顯示:CAP 聯合化療組的中位生存期、疾病無進展生存期和治療總有效率明顯優于對照組;但兩組在 1 年生存率方面差異無統計學意義。在毒副作用方面,CAP 聯合化療組 3~4 級中性粒細胞減少、口腔炎及手足綜合征的發生率高于對照組。對于 CAP 聯合方案未能提高患者 1 年生存率的原因可能為:首先 PC 惡性程度極高,本研究納入均為晚期 PC 患者,生存期均較短;其次樣本量小,僅 3 個研究報道了 664 例患者 1 年生存率情況,仍需更多樣本量的研究來驗證結果。
近年來靶向治療是腫瘤治療的新希望,但近期關于晚期 PC 靶向治療的臨床試驗均以失敗告終。凡德他尼聯合 GEM 未改善晚期胰腺癌患者生存情況[14];厄洛替尼雖被證實聯合 GEM 可改善局部進展和(或)轉移性胰腺癌患者預后,但生存獲益有限[15];循證醫學證據也表明不同靶向治療聯合 GEM 并未改善晚期胰腺癌患者生存狀況[16]。本研究結果顯示 CAP 聯合化療組的中位生存期、疾病無進展生存期明顯長于對照組。在毒副作用方面,兩方案均顯示了常見的血液學及非血液毒性;但 CAP 聯合化療方案的中性粒細胞減少、口腔炎及手足綜合征的發生率明顯高于對照組。因此在使用 CAP 聯合化療中需注意監測患者血常規,及時了解中性粒細胞變化情況,注意預防口腔炎及手足綜合征的發生。對于存在腹腔轉移的 PC 患者,Satoi 等[17]報道了靜脈和腹腔注射紫杉醇聯合 S-1 治療胰腺癌腹腔轉移,結果顯示患者的中位總生存期為 16.3 個月,1 年生存率為 62%,有效率與疾病控制率分別為 36% 和 82%,但該方案的有效性和安全性仍有待更多臨床試驗驗證。
本系統評價仍然存在一定的局限性:① 部分研究未采用正確的隨機分配和隱藏方法,可能造成選擇性偏倚。② 未納入非中、英文文獻,可能存在發表偏倚,故要想獲得確鑿的證據尚需要擴大樣本,長期隨訪。
綜上所述,CAP 聯合應用可能改善進展期胰腺癌病人的短期生存情況及生活質量;但會導致部分毒副反應增加,且 1 年以后的遠期生存無明顯改善。
胰腺癌(pancreatic cancer,PC)是惡性程度最高的消化系統腫瘤。由于其早期缺乏特異性的臨床表現,大多患者因癥狀出現就診時腫瘤已經擴散或轉移,確診后 5 年生存率低于 8%[1]。PC 近年來在全球范圍內均呈快速上升趨勢。2018 年美國預計新發 PC 患者 5.5 萬例,因其死亡人數達 4.4 萬例[2];預計到 2030 年,PC 將成為美國第二大癌癥死亡原因[3]。我國國家癌癥中心發布的最新數據也顯示中國 PC 發病率上升到惡性腫瘤的第十位,癌癥相關死亡率位于第六位[1]。雖然普通人群的體檢意識不斷增強,診斷技術不斷提高,但大部分 PC 發現時已是不可切除的晚期。中國的《PC 診治指南(2014)》指出對于不可切除的局部進展期或轉移性胰腺癌,積極的化學治療有助于緩解癥狀,延長生存期及改善生活質量;并推薦使用以吉西他濱(gemcitabine,GEM)為基礎的化療方案[4]。近年來已有研究[5, 6]表明 GEM 聯合化療優于標準的 GEM 單藥化療,GEM 聯合化療將是今后治療 PC 的希望與方向。同時,與卡培他濱(capecitabine,CAP)相關的進展期 PC 化療臨床試驗亦廣泛開展,而不同研究結論尚存在差異[7, 8]。本研究旨在系統評價 CAP 聯合 GEM 化療是否能在毒副反應可控的前提下顯著提高進展期 PC 的治療效果,為臨床治療胰腺癌提供參考。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型
CAP 聯合化療方案與非 CAP 聯合化療方案治療晚期 PC 的隨機對照試驗(RCT)。
1.1.2 研究對象
① 均是經病理學或細胞學檢查證實的Ⅲ~Ⅳ期(進展期或轉移)胰腺癌患者;② 年齡≥18 歲,性別不限;③ ECOG 評分為 0~2 分,或 Kamofsky 評分≥60 分。
1.1.3 干預措施
試驗組采用 CAP 聯合方案治療;非 CAP 聯合化療方案采用 GEM 單藥或含 GEM 的聯合方案治療。兩組除試驗組含 CAP 外,其他化療藥物在兩組間一致。
1.1.4 結局指標
① 中位生存期;② 疾病無進展生存期;③ 治療總有效率(CR+PR);④ 1 年生存率;⑤ 3~4 級毒副反應。
1.1.5 排除標準
① 非中、英文文獻;② 同時患第二種惡性腫瘤者;③ 1 個月內接受其他的抗癌治療;④ 預計生存期<3 個月者。
1.2 文獻檢索策略
計算機檢索 PubMed、The Cochrane Library、WanFang Data 和 CNKI 數據庫,搜集 CAP 聯合化療方案與不含 CAP 的化療方案比較治療晚期 PC 的 RCT,檢索時限均從建庫至 2017 年 12 月 1 日。此外,追溯納入文獻的參考文獻,以補充獲取相關文獻。檢索采取主題詞和自由詞相結合的方式。英文檢索詞包括:gemcitabine、capecitabine、pancreatic cancer、pancreatic carcinoma;中文檢索詞包括:吉西他濱、卡培他濱、胰腺癌。以 PubMed 為例,其具體檢索策略見框 1。

1.3 文獻篩選和資料提取
由 2 位評價員獨立篩選文獻、提取資料并交叉核對,如遇分歧,則咨詢第三方協助判斷,缺乏的資料盡量與作者聯系予以補充。文獻篩選時首先閱讀文題和摘要,在排除明顯不相關的文獻后,進一步閱讀全文,以確定最終是否納入。資料提取內容主要包括:① 納入研究的基本信息,包括研究題目、第一作者、發表雜志和時間等;② 研究對象的基線特征,包括各組樣本數、患者年齡、性別和疾病狀況等;③ 干預措施的具體細節、隨訪時間等;④ 偏倚風險評價的關鍵要素;⑤ 所關注的結局指標和結果測量數據。
1.4 納入研究的偏倚風險評價
由 2 名評價員按照 Cochrane 手冊針對 RCT 的偏倚風險評價工具評價納入研究的偏倚風險[9]。
1.5 統計分析
采用 RevMan 5.3 軟件進行 Meta 分析。采用 RR 和 HR 作為效應指標,各效應量均給出其點估計值和 95%CI。納入研究結果間的異質性采用 χ2 檢驗進行分析(檢驗水準為 α=0.1),同時結合 I2 定量判斷異質性的大小。若各研究結果間無統計學異質性,則采用固定效應模型進行 Meta 分析;若各研究結果間存在統計學異質性,則進一步分析異質性來源,在排除明顯臨床異質性的影響后,采用隨機效應模型進行 Meta 分析。明顯的臨床異質性采用亞組分析或敏感性分析等方法進行處理,或只行描述性分析。Meta 分析的檢驗水準設為 α=0.05。
2 結果
2.1 文獻篩選流程及結果
初檢出相關文獻 493 篇,經逐層篩選后,最終納入 6 個 RCT[7, 8, 10-13],共 1 317 例患者。文獻篩選流程及結果見圖 1。
 圖1
文獻篩選流程及結果
圖1
文獻篩選流程及結果
*所檢索的數據庫及檢出文獻數具體如下:PubMed(
2.2 納入研究的基本特征與偏倚風險評價結果
2.3 Meta 分析結果
2.3.1 中位生存期
共納入 5 個 RCT[7, 8, 10-12]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的中位生存期明顯優于對照組,差異有統計學意義[HR=0.86,95%CI(0.77,0.96),P=0.006](表 3)。
2.3.2 疾病無進展生存期
共納入 5 個 RCT[7, 8, 10-12]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的疾病無進展生存期明顯優于對照組,差異有統計學意義[HR=0.83,95%CI(0.75,0.91),P=0.000 2](表 3)。
2.2.3 治療總有效率
共納入 6 個 RCT[7, 8, 10-13]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的治療總有效率明顯高于對照組,差異有統計學意義[RR=1.64,95%CI(1.27,2.11),P=0.000 1](表 3)。
2.2.4 1 年生存率
共納入 3 個 RCT[10, 12, 13]。固定效應模型 Meta 分析結果顯示,兩組 1 年總生存率的差異無統計學意義[RR=1.08,95%CI(0.83,1.40),P=0.58](表 3)。
2.2.5 3~4 級毒副作用
共納入 6 個 RCT[7, 8, 10-13]。固定效應模型 Meta 分析結果顯示,CAP 聯合化療組的 3~4 級中性粒細胞減少、口腔炎及手足綜合征的發生率高于非 CAP 聯合化療組(P 均<0.05)。兩組在 3~4 級貧血、血小板減少、乏力、惡心嘔吐及腹瀉方面的差異無統計學意義(P 均>0.05)(表 4)。
3 討論
晚期 PC 患者的生存時間短,目前最適合的化療方案仍不明確,急需尋找有效的化療藥物方案改善預后。以 GEM 為基礎的化療藥物治療 PC 的臨床效果確切,并為美國國立綜合癌癥網絡(NCCN)的 PC 診療指南及中國的《PC 診治指南(2014)》所推薦[4];對于不可切除的局部進展期或轉移性 PC,在全身狀況良好的情況下,采用以 GEM 或氟尿嘧啶類藥物為基礎的同步放化療或誘導化療后放療可有效緩解癥狀及改善患者預后[4]。近年來有研究報道 CAP 聯合 GEM 化療方案能夠延長晚期 PC 患者的疾病無進展生存期,但部分研究結果并不一致;因此我們將相關研究結果進行了系統評價。
本研究共納入 6 個 RCT,含 1 317 例晚期 PC 患者。Meta 分析結果顯示:CAP 聯合化療組的中位生存期、疾病無進展生存期和治療總有效率明顯優于對照組;但兩組在 1 年生存率方面差異無統計學意義。在毒副作用方面,CAP 聯合化療組 3~4 級中性粒細胞減少、口腔炎及手足綜合征的發生率高于對照組。對于 CAP 聯合方案未能提高患者 1 年生存率的原因可能為:首先 PC 惡性程度極高,本研究納入均為晚期 PC 患者,生存期均較短;其次樣本量小,僅 3 個研究報道了 664 例患者 1 年生存率情況,仍需更多樣本量的研究來驗證結果。
近年來靶向治療是腫瘤治療的新希望,但近期關于晚期 PC 靶向治療的臨床試驗均以失敗告終。凡德他尼聯合 GEM 未改善晚期胰腺癌患者生存情況[14];厄洛替尼雖被證實聯合 GEM 可改善局部進展和(或)轉移性胰腺癌患者預后,但生存獲益有限[15];循證醫學證據也表明不同靶向治療聯合 GEM 并未改善晚期胰腺癌患者生存狀況[16]。本研究結果顯示 CAP 聯合化療組的中位生存期、疾病無進展生存期明顯長于對照組。在毒副作用方面,兩方案均顯示了常見的血液學及非血液毒性;但 CAP 聯合化療方案的中性粒細胞減少、口腔炎及手足綜合征的發生率明顯高于對照組。因此在使用 CAP 聯合化療中需注意監測患者血常規,及時了解中性粒細胞變化情況,注意預防口腔炎及手足綜合征的發生。對于存在腹腔轉移的 PC 患者,Satoi 等[17]報道了靜脈和腹腔注射紫杉醇聯合 S-1 治療胰腺癌腹腔轉移,結果顯示患者的中位總生存期為 16.3 個月,1 年生存率為 62%,有效率與疾病控制率分別為 36% 和 82%,但該方案的有效性和安全性仍有待更多臨床試驗驗證。
本系統評價仍然存在一定的局限性:① 部分研究未采用正確的隨機分配和隱藏方法,可能造成選擇性偏倚。② 未納入非中、英文文獻,可能存在發表偏倚,故要想獲得確鑿的證據尚需要擴大樣本,長期隨訪。
綜上所述,CAP 聯合應用可能改善進展期胰腺癌病人的短期生存情況及生活質量;但會導致部分毒副反應增加,且 1 年以后的遠期生存無明顯改善。