四川大學華西醫院腫瘤生物治療研究室陳俐娟研究員團隊2016年6月發表于Nature Communications的文章"Pironetin reacts covalently with cysteine-316 of a-tubulin to destabilize microtubule"(影響因子:12.353)(長按下方二維碼即可閱讀原文)。

微管(Microtubule)是抗腫瘤藥物研發的重要靶點。微管是“細胞骨架”的主要成分之一,在許多細胞重要事件中起著關鍵作用。微管是由α-和β-微管蛋白(Tubulin)異二聚體可逆地組裝而成的線性管裝結構(圖 1a)。
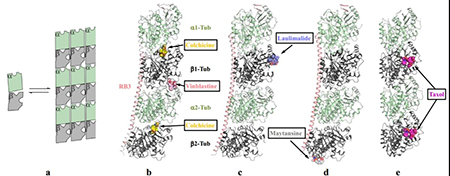
圖1 微管和微管蛋白的結構。(a)微管蛋白二聚體從頭到尾排列形成微管,其構象由彎曲變直,二聚體之間同時縱向和橫向接觸。(b-e)微管與已知 5 個位點之間的相互結合圖:(b)長春堿和秋水仙堿結合于 β-tubulin 的具體位點;(c)微管聚合劑Laulimalide 在 β-tubulin 上的結合位點;(d)微管抑制劑美登木素在 β-tubulin 上的結合位點;(e)微管聚合劑在 β-tubulin 上的結合位點。蛋白由 cartoon 形式表示,小分子用球形模式表示
天然產物長春花堿、秋水仙堿、紫杉醇、laulimalide 和美登素都與 β-微管蛋白結合并干擾其正常動力學過程從而抑制微管蛋白的聚合或解聚:長春堿、秋水仙堿和美登素抑制微管蛋白異二聚體聚合形成微管,而紫杉醇和 laulimalide 促進聚合和穩定微管。結構生物學詳細描述了這五種天然化合物如何結合并改變 β-微管蛋白的構象從而改變微管和微管之間的動力學特征(如圖 1b-e)。 這些工作使得新一代理性設計微管抑制劑成為可能,極大地有助于微管藥物的開發。紫杉醇代表了最成功的一類在臨床使用的抗腫瘤藥物,目前其全球銷售額已經超過300億美元。但是,在病人進行治療時, βIII-微管蛋白的表達會增加,這種微管蛋白與紫杉醇的結合很弱,這種突變的微管蛋白能夠抵抗紫杉醇的治療從而產生耐藥性。
Pironetin是一個天然小分子,是目前報道的唯一與α-微管蛋白相互作用的小分子。其展示了良好的體內外抗腫瘤活性,同時在多藥耐藥細胞上同樣有效。日本的研究人員通過詳盡的實驗方法證明Pironetin結合于α-微管蛋白的352位賴氨酸。在他們的研究中明確說明了Pironetin不會與半胱氨酸結合。但不幸的是,基于 K352 的Pironetin結合模型給Pironetin衍生物的設計帶來了困難,多數研究都顯示,改造以后Pironetin活性明顯下降。因此,鑒于 Pironetin衍生物的修飾合成沒有取得進展, Piroentin 衍生物的設計就此被擱置了。但是,開發靶向 α-微管蛋白的藥物仍然具有巨大開發價值。這種新型的靶向α-微管蛋白的藥物很可能不受 β-微管蛋白的突變及 βIII-微管蛋白的高表達所影響,從而其在耐藥細胞上也會有效。四川大學華西醫院腫瘤生物治療研究室陳俐娟課題組一直從事抗微管藥物研發,為了推進靶向 α-tubulin 抑制劑的開發,該課題組對Pironetin與微管蛋白的相互作用進行深入的研究,獲得了與之前的研究完全不同的結果。通過結構生物學及質譜實驗結果顯示,Pironetin 確實是結合在α-微管蛋白上,但是其共價結合的位點為 316 位半胱氨酸,而不是 352 位賴氨酸(圖2)。
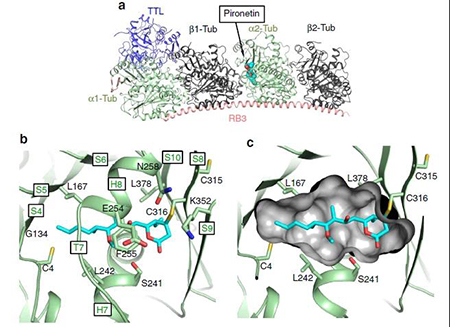
圖2 微管蛋白-RB3-TTL-Pironetin復合物的結構。(a)Pironetin-微管蛋白-RB3-TTL的結構。(b)Pironetin在α-微管蛋白單體的口袋中的近視圖。 (c)Pironetin結合口袋表面的橫截面圖
同時通過生物質譜實驗更進一步證實了Pironetin結合于α-微管蛋白的316位半胱氨酸。如圖3所示,該肽段的二級質譜碎片顯示Pironetin結合于 Cys316。
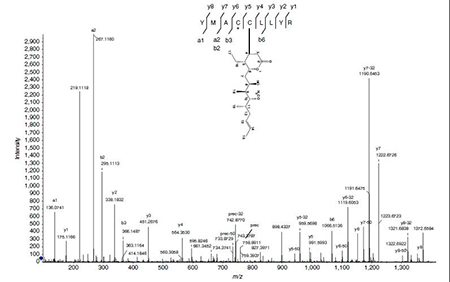
圖3 α-微管蛋白的Pironetin共價修飾的肽段的MS / MS二級碎裂質譜圖
在總體水平上,Pironetin與α2-微管蛋白亞基的結合導致了 α1β1 異二聚體相對于α2β2異二聚體之間約2°的旋轉(圖4a)。在二級結構層面造成了明顯的T7 loop環的偏移(殘基Phe244至Leu259的變化):Val250的Cα原子移動超過11?,而 Leu252和Gly246已經分別偏移了6?和8?(圖 4b)。為了適應 Pironetin的結合,Cys316兩側的殘鏈S8不同側鏈都有小的位移(圖4c)。Glu254在空白結構中是關鍵的催化殘基,Glu254與水分子結合,水分子又與鄰近的 β1-微管蛋白的 Mg2+離子結合(圖4c),而 Mg2+ 離子又與 GDP 的磷酸鹽接觸,從而調控GTP水解。Pironetin導致的Glu254位置的偏移所造成的β-微管蛋白的GTPase活性降低(圖 4c-d)可能是另外的Pironetin抑制微管聚合的機制。至此作者詳細地解釋了Pironetin與α-微管蛋白的相互作用,為后續開發靶向α-微管蛋白的藥物奠定了基礎。

圖4 Pironetin結合導致微管結構的變化。(a)apo形式和與Pironetin結合的復合物中的微管蛋白結構的比較。(b)apo蛋白形式(藍色)和復合物形式蛋白中(綠色)H8的主要主鏈變化。(c)α-微管蛋白的催化殘基E254與銜接頭結合上的F255一起重新定向。(d)Pironetin抑制微管蛋白的GTPase活性,與長春堿類似,與秋水仙堿相反
專家點評
程偉教授:微管是抗腫瘤藥物研發的熱點,臨床上市的藥物如紫杉醇,長春堿及艾日布林等均靶向β-微管蛋白,但β-微管蛋白容易突變而導致耐藥性的產生。相對而言,α-微管蛋白不易突變,是一個更好的抗腫瘤靶蛋白。因此開發靶向 α-微管蛋白的抗腫瘤藥物具有重要的研究價值。但目前為止僅有一個天然小分子Pironetin被報道共價結合于 α-微管蛋白。但是其結合位點等相關機制仍然不清楚。陳俐娟研究員課題組長期致力于抗腫瘤微管蛋白抑制劑的研究,成功解析了Pironetin-微管蛋白復合物的晶體結構,發現了Pironetin的結合位點為α-微管蛋白的316位半胱氨酸,成功解釋了Pironetin的作用機制。他們報道了一個全新的靶向α-微管蛋白的小分子結合位點,對于后續開發靶向α-微管蛋白的新型微管抑制劑具有重要意義。

程偉,博士,四川大學華西醫院生物治療國家重點實驗室教授。主要針對重大疾病(如癌癥、感染性疾病)進行藥物靶標發現、驗證及結構和功能研究,主要利用X-ray和cryo-EM技術,結合生物化學、遺傳學及細胞生物學從事蛋白質機器研究。以通訊作者或第一作者(包括共同) 在Science、Nature子刊、Cell子刊等國際高影響力期刊發表論文數篇。程教授目前主持四川大學、四川大學華西醫院及國家自然科學基金委員會等項目;榮獲2014美國“Judith Graham Pool Postdoctoral Research ”獎項。
作者投稿心得
該文章從最開始發現到最后文章見刊發表僅用了一年半時間,是與各領域的專家合作才能達到如此高的效率。在通訊作者陳俐娟研究員的統籌指導下:共同第一作者楊建洪、王太津負責藥理及計算機輔助設計等實驗;王譽熹、蔣健負責結構生物學實驗;共同通訊作者朱曉峰負責晶體結構解析,同時邀請了英國皇家科學院院士James H. Naismith參與文章的撰寫指導。該文章的快速發表充分體現了合作及協同創新在科研中的重要作用。
作者
博士后楊建洪、王譽熹,博士生王太津及碩士生蔣健為共同第一作者,四川大學華西醫院陳俐娟研究員與四川大學生命科學院朱曉峰教授為通訊作者
通信作者

陳俐娟,博士,四川大學二級教授,博士生導師,博士后合作導師,四川大學華西醫院生物治療國家重點實驗室副主任,教育部新世紀優秀人才獲得者,2017年度“藥明康德生命化學研究獎”獲得者。現任中華中醫聯盟協會會員,中國醫藥生物技術協會納米生物專業委員會理事;《四川大學學報醫學版》編委;中國西部有機質譜委員會副理事長;四川省生物技術協會副理事長;四川省靶向抗癌學會副理事長。長期從事天然藥物小分子和靶向小分子的藥物開發研究,作為項目/課題負責人主持完成20余項國家及省部級科研項目,包括國家863重大項目1項,重大新藥創制5項,國家自然科學基金儀器重大專項1項,自然科學基金聯合基金重點項目1項,面上項目5項。在Nature Communication、Journal of Medicinal Chemistry、Biomaterial、Journal of Controlled Release等期刊以通訊作者身份發表 SCI 收錄論文200余篇,申請美、英、德、中等國家發明專利50余項,其中授權專利25項。經過多年積累,其研究團隊成果成功實施轉化,目前有多個候選化合物已進入臨床前評價,1個國家天然產物一類創新藥物已進入I期臨床,1個國家一類創新藥物申報臨床研究。
通信作者

朱曉峰,四川大學生命科學學院教授,2006年6月獲英國斯特拉思克萊德大學和格拉斯哥大學聯合授予的生物科學博士學位。博士畢業至2012年9月在英國圣安德魯斯大學從事研究工作6年,參與了多項由英國生物技術研究委員會(BBSRC)資助的酶學和結構生物學研究重大項目。2012年10月回四川大學生命科學學院工作,主要以天然產物生物合成途徑中具有特殊催化功能的酶為研究對象,開展酶晶體結構和催化反應機理的研究,以通訊作者或第一作者發表文章在Nat Commun、JACS、JBC、JMB等學術期刊上。
版權聲明:華西微家倡導尊重和保護知識產權。歡迎轉載、引用,但需取得本平臺授權。如您對文章內容版權存疑,請致電028-85422587,我們會與您及時溝通處理。本站內容及圖片僅供參考、學習使用,不為盈利且不作為診斷、醫療根據。
本文編輯:張 敏
本文排版:陳紅梅 張洪雪